Page 76 - 化学魔法师入门手册
P. 76
上海大学附属中学校本课程 化学魔法师入门手册——创新实践篇
验现象→得出结论→原理。
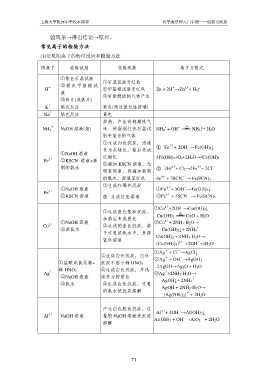
常见离子的检验方法
(1)常见阳离子的特征反应和检验方法
阳离子 检验试剂 实验现象 离子方程式
①紫色石蕊试液
①石蕊试液变红色
②橙色 甲基 橙试
+
2 +
H + ②甲基橙试液变红色 Zn + 2H →Zn + H2↑
液
③有能燃烧的气体产生
③锌片(或铁片)
K + 焰色反应 紫色(透过蓝色钴玻璃)
Na + 焰色反应 黄色
加热,产生有刺激性气
+ + -
NH4 NaOH 溶液(浓) 味、使湿润红色石蕊试 NH4 + OH NH3↑+ H2O
纸变蓝色的气体
①生成白色沉淀,迅速
-
① Fe 2 + + 2OH →Fe(OH)2↓
变为灰绿色,最后变成
①NaOH 溶液 红褐色 4Fe(OH)2+O2+2H2O→4Fe(OH)3
Fe 2 + ②KSCN 溶液+新
②滴加 KSCN 溶液,无
制的氯水 ② 2Fe + Cl2→2Fe + 2Cl -
2 +
3 +
明显现象,再滴加新制
-
的氯水,溶液呈红色 Fe 3 + + 3SCN → Fe(SCN)3
①生成红褐色沉淀
-
①NaOH 溶液 ①Fe 3 + + 3OH →Fe(OH)3↓
Fe 3 +
-
②KSCN 溶液 ③ 生成红色溶液 ②Fe 3 + + 3SCN → Fe(SCN)3
-
2 +
①Cu +2OH →Cu(OH)2↓
①生成蓝色絮状沉淀,
Cu(OH)2 CuO + H2O
加热后变成黑色
2 +
①NaOH 溶液 ②Cu + 2NH3·H2O→
Cu 2 + ②生成的蓝色沉淀,溶 +
②浓氨水 Cu(OH)2↓+ 2NH4
于过量浓氨水中,呈深
Cu(OH)2 + 4NH3·H2O→
蓝色溶液
2 +
-
[Cu(NH3)4] +2OH +4H2O
-
+
①Ag + Cl →AgCl↓
①生成白色沉淀,白色 + -
①盐酸或氯化物+ 沉淀不溶于稀 HNO3 ②Ag + OH →AgOH↓
2AgOH→Ag2O + H2O
稀 HNO3 ②生成白色沉淀,并迅
+
Ag + ③Ag +2NH3·H2O→
②NaOH 溶液 速变为棕黑色 +
AgOH↓+ 2NH4
③氨水 ③生成白色沉淀,过量
AgOH + 2NH3·H2O→
的氨水使沉淀溶解
[Ag(NH3)2] + 2H2O
+
产生白色胶状沉淀,过 Al + 3OH →Al(OH)3↓
-
3 +
Al 3 + NaOH 溶液 量的 NaOH 溶液使沉淀
-
-
Al(OH)3 + OH →AlO2 + 2H2O
溶解
71